「大量出血」という合併症
MIFEPREX safely and effectively. See full prescribing information for MIFEPREX.
関連するところを仮訳と原文で示します。最後まで……というか、ぜひ最後を見てください!
HIGHLIGHTS OF PRESCRIBING INFORMATION These highlights do not include all the information needed to use MIFEPREX safely and effectively. See full prescribing information for MIFEPREX. MIFEPREX® (mifepristone) tablets, for oral use Initial U.S. Approval: 2000
最初に出てくるBoxの警告
警告:重篤な、時に致命的な感染症や出血
完全なBox警告については、完全な処方情報を参照してください。
重篤な、時には致命的な感染症や出血が、自然流産、外科的流産、薬による流産(ミフェックスの使用後も含む)の後に、ごく稀に発生します。【引用者注:薬による中絶が感染症や出血の原因であるとは言っておらず、流産後や外科的または内科的中絶後に、重篤で時に致命的な感染症や出血が起こることがまれだがありうると言っているのです。】
- 感染症の非典型的な症状。重篤な細菌感染症や敗血症の患者は、発熱、菌血症、または内診検査で重要な所見が見られなくても発症することがあります。重篤な感染症や敗血症を除外するには、慎重に判断する必要があります。(5.1)
- 出血。長引く多量の出血は、不完全な中絶やその他の合併症の兆候である可能性があり、迅速な医学的または外科的介入が必要となる場合があります。(5.2)
MIFEPREXは、MIFEPREX REMSプログラムと呼ばれる制限付きプログラムを通じてのみ入手可能です(5.3)。
MIFEPREXを処方する前に、これらのリスクについて患者に伝えてください。
持続的な発熱、激しい腹痛、長期にわたる大量出血、失神を経験した場合、あるいはミソプロストール服用後24時間以上にわたって腹痛や不快感、全身倦怠感を経験した場合、誰に連絡し、何をすべきかを患者に確認してください。
患者が緊急治療室や、マイフェックスを処方していない他の医療機関を訪れる際には、薬による中絶を行っていることを医療機関に知ってもらうために、薬用ガイドを持っていくように助言してください。(5.1, 5.2)
WARNING: SERIOUS AND SOMETIMES FATAL INFECTIONS OR
BLEEDING
See full prescribing information for complete boxed warning.
Serious and sometimes fatal infections and bleeding occur very rarely following spontaneous, surgical, and medical abortions, including following MIFEPREX use.
• Atypical Presentation of Infection. Patients with serious bacterial
infections and sepsis can present without fever, bacteremia or significant findings on pelvic examination. A high index of suspicion is needed to rule out serious infection and sepsis. (5.1)
• Bleeding. Prolonged heavy bleeding may be a sign of incomplete abortion or other complications and prompt medical or surgical intervention may be needed. (5.2)
MIFEPREX is only available through a restricted program called the MIFEPREX REMS Program (5.3).
Before prescribing MIFEPREX, inform the patient about these risks.
Ensure the patient knows whom to call and what to do if she experiences
sustained fever, severe abdominal pain, prolonged heavy bleeding, or
syncope, or if she experiences abdominal pain or discomfort or general
malaise for more than 24 hours after taking misoprostol.
Advise the patient to take the MEDICATION GUIDE with her if she
visits an emergency room or another healthcare provider who did not
prescribe MIFEPREX, so that provider knows that she is undergoing a
medical abortion. (5.1, 5.2)
6 副作用
以下の副作用については、他の項で詳しく説明しています。- 感染症及び敗血症[警告及び注意(5.1)参照] - 子宮出血[警告及び注意(5.2)参照] 6.1 臨床試験の経験 臨床試験は様々な条件下で実施されるため、ある薬剤の臨床試験で観察された副作用の割合を他の薬剤の臨床試験の割合と直接比較することはできず、実際に観察された割合を反映していない可能性がある。一般的な副作用に関する情報は、米国で実施された試験のデータのみに基づいています。米国以外の試験で報告された副作用の発現率は著しく低く、米国の人口に一般化できない可能性があるためです。ミフェプリストン200mgを経口投与し、その24~48時間後にミソプロストール800mcgを頬投与した妊娠70日までの女性1,248人を対象とした米国の3つの臨床試験では、女性は日記や追跡調査時のインタビューで副作用を報告しました。これらの試験では、ミフェプリストンまたはミソプロストールの使用が禁忌ではない、生殖可能な年齢の一般的に健康な女性が登録されました(MIFEPREXの製品ラベルによる)。6 ADVERSE REACTIONS
The following adverse reactions are described in greater detail in other sections: - Infection and sepsis [see Warnings and Precautions (5.1)] - Uterine bleeding [see Warnings and Precautions (5.2)] 6.1 Clinical Trials Experience Because clinical studies are conducted under widely varying conditions, adverse reaction rates observed in the clinical studies of a drug cannot be directly compared to rates in the clinical studies of another drug and may not reflect the rates observed in practice. Information presented on common adverse reactions relies solely on data from US studies, because rates reported in non-US studies were markedly lower and are not likely generalizable to the US population. In three US clinical studies totaling 1,248 women through 70 days gestation who used mifepristone 200 mg orally followed 24-48 hours later by misoprostol 800 mcg buccally, women reported adverse reactions in diaries and in interviews at the follow-up visit. These studies enrolled generally healthy women of reproductive age without contraindications to mifepristone or misoprostol use according to the MIFEPREX product label.
警告:重篤な、時には致命的な感染症や出血
自然流産、外科的流産、薬による流産に伴い、重篤な、時には致命的な感染症や出血が非常に稀に発生します(MIFEPREX使用後を含む)。MIFEPREXやミソプロストールの使用とこれらの事象との因果関係は確立されていません。
- 感染症の非典型的な症状。重篤な細菌感染症(例えば、Clostridium sordellii)や敗血症の患者は、中絶後に発熱や菌血症、骨盤検査で目立った所見がなくても来院することがあります。ごくまれに、発熱がなく、腹痛があるかないかにかかわらず、著しい左シフトを伴う白血球増加、頻脈、血液濃縮、全身倦怠感を呈した患者の死亡例が報告されています。重篤な感染症や敗血症を除外するためには、高い疑義が必要です[「警告および注意」(5.1)参照]。
- 出血。長引く大量出血は、不完全な中絶またはその他の合併症の徴候である可能性があり、迅速な医学的または外科的介入が必要となる場合があります。長引く大量の膣内出血を経験した場合には、直ちに医師の診察を受けるように患者に助言してください[「警告と注意」(5.2)参照]。上記のような重篤な合併症のリスクがあるため、MIFEPREXはMIFEPREX REMSプログラムと呼ばれるリスク評価・緩和戦略(REMS)に基づく制限付きプログラムを通じてのみ入手可能です[「警告と注意」(5.3)参照]。MIFEPREXを処方する前に、これらの重篤なイベントのリスクについて患者に伝えてください。患者が、提供された連絡先のいずれにも連絡がつかない場合、持続的な発熱、激しい腹痛、長期にわたる大量出血、失神を経験した場合、あるいはミソプロストール服用後24時間以上、腹痛や不快感、全身倦怠感(脱力感、吐き気、嘔吐、下痢を含む)を経験した場合に、緊急治療室に行くことを含め、誰に連絡し、何をすべきかを知っていることを確認してください。患者が緊急治療室やマイフェックスを処方していない医療機関を訪れる際には、薬による中絶を行っていることを医療機関に知ってもらうために、メディケーション・ガイドを持っていくように助言してください。
WARNING: SERIOUS AND SOMETIMES FATAL INFECTIONS OR BLEEDING
Serious and sometimes fatal infections and bleeding occur very rarely following spontaneous, surgical, and medical abortions, including following MIFEPREX use. No causal relationship between the use of MIFEPREX and misoprostol and these events has been established. • Atypical Presentation of Infection. Patients with serious bacterial infections (e.g., Clostridium sordellii) and sepsis can present without fever, bacteremia, or significant findings on pelvic examination following an abortion. Very rarely, deaths have been reported in patients who presented without fever, with or without abdominal pain, but with leukocytosis with a marked left shift, tachycardia, hemoconcentration, and general malaise. A high index of suspicion is needed to rule out serious infection and sepsis [see Warnings and Precautions (5.1)]. • Bleeding. Prolonged heavy bleeding may be a sign of incomplete abortion or other complications and prompt medical or surgical intervention may be needed. Advise patients to seek immediate medical attention if they experience prolonged heavy vaginal bleeding [see Warnings and Precautions (5.2)]. Because of the risks of serious complications described above, MIFEPREX is available only through a restricted program under a Risk Evaluation and Mitigation Strategy (REMS) called the MIFEPREX REMS Program [see Warnings and Precautions (5.3)]. Before prescribing MIFEPREX, inform the patient about the risk of these serious events. Ensure that the patient knows whom to call and what to do, including going to an Emergency Room if none of the provided contacts are reachable, if she experiences sustained fever, severe abdominal pain, prolonged heavy bleeding, or syncope, or if she experiences abdominal pain or discomfort, or general malaise (including weakness, nausea, vomiting or diarrhea) for more than 24 hours after taking misoprostol. Advise the patient to take the Medication Guide with her if she visits an emergency room or a healthcare provider who did not prescribe MIFEPREX, so that the provider knows that she is undergoing a medical abortion.
5.2 子宮の出血
子宮の出血は、薬による中絶を行っているほとんど全ての患者に起こります。長引く大量の出血(厚手のフルサイズの生理用ナプキン2枚が1時間に2時間連続で浸るほど)は、不完全な中絶やその他の合併症の兆候である可能性があり、血液量減少性ショックの発生を防ぐために、迅速な医学的または外科的な介入が必要となります。薬による中絶後に長期にわたる大量の膣からの出血を経験した場合は、直ちに医師の診察を受けるように患者に助言してください[箱入り警告を参照]。女性は、平均して9日から16日の間、膣からの出血や点状出血を経験することになります。女性は、中央値で2日間の大量出血を経験したと報告しています。全被験者の最大8%が30日以上にわたって何らかの出血を経験する可能性があります。一般的に、妊娠期間が長くなるにつれて、出血や点状出血の期間が長くなりました。大量に出血した女性では、ヘモグロビン濃度、ヘマトクリット、赤血球数の減少が起こる可能性があります。過度の子宮出血は,通常,子宮栄養剤,血管収縮剤,外科的な子宮の摘出,生理食塩水の投与,および/または輸血による治療を必要とします。いくつかの大規模臨床試験のデータによると、血管収縮剤は全被験者の4.3%に使用され、5.5%の被験者で2g/dL以上のヘモグロビン低下が見られ、0.1%以下の被験者に輸血が行われました。文献ID:3909592 5 外科的な子宮摘出を必要とする大出血は約1%の患者に起こるため、止血障害、低凝固性、重度の貧血のある患者には特に注意を払う必要がある。
5.2 Uterine Bleeding Uterine bleeding occurs in almost all patients during a medical abortion. Prolonged heavy bleeding (soaking through two thick full-size sanitary pads per hour for two consecutive hours) may be a sign of incomplete abortion or other complications and prompt medical or surgical intervention may be needed to prevent the development of hypovolemic shock. Counsel patients to seek immediate medical attention if they experience prolonged heavy vaginal bleeding following a medical abortion [see Boxed Warning]. Women should expect to experience vaginal bleeding or spotting for an average of 9 to 16 days. Women report experiencing heavy bleeding for a median duration of 2 days. Up to 8% of all subjects may experience some type of bleeding for 30 days or more. In general, the duration of bleeding and spotting increased as the duration of the pregnancy increased. Decreases in hemoglobin concentration, hematocrit, and red blood cell count may occur in women who bleed heavily. Excessive uterine bleeding usually requires treatment by uterotonics, vasoconstrictor drugs, surgical uterine evacuation, administration of saline infusions, and/or blood transfusions. Based on data from several large clinical trials, vasoconstrictor drugs were used in 4.3% of all subjects, there was a decrease in hemoglobin of more than 2 g/dL in 5.5% of subjects, and blood transfusions were administered to ≤ 0.1% of subjects. Because heavy bleeding requiring Reference ID: 3909592 5 surgical uterine evacuation occurs in about 1% of patients, special care should be given to patients with hemostatic disorders, hypocoagulability, or severe anemia.
では、どれだけの「大出血」があるのかといえば、次の表。
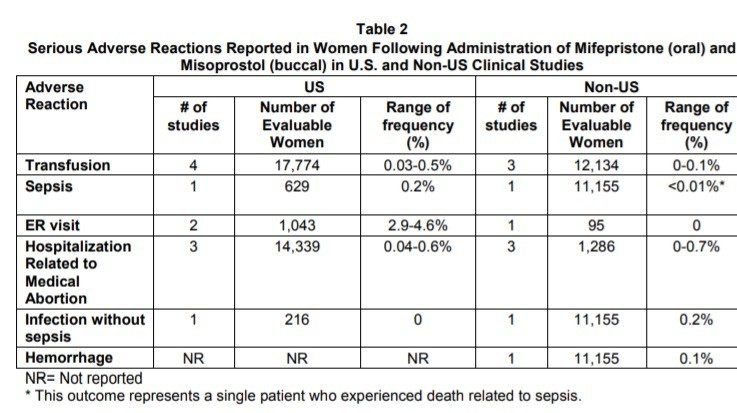
大出血(hemorage)については、アメリカ国内では皆無で、国外の1つの研究のみ0.1%となっているんですね。薬のせいというよりも、他に原因があるのでは……と疑ってしまう。